Melflufen (melphalan flufenamid) er et nyt lægemiddel, der undersøges i behandlingen af recidiverende eller ildfast multipelt myelom (RRMM). Det er et derivat af kemoterapimedicinen melphalan. Melflufen er et peptid-lægemiddelkonjugat; en kombination af melphalan og et peptid (lille protein) bundet sammen. Melflufen gives ved intravenøs infusion (i venen).
Lægemidlet blev indsendt som en ny lægemiddelansøgning til US Food and Drug Administration (FDA) i juli 2020. FDA godkendte ansøgningen prioriteret gennemgang, og en beslutning forventes i slutningen af februar 2021. Melflufen er endnu ikke bredt tilgængelig, fordi det ikke er licenseret og godkendt til brug i myelom. Imidlertid kan patienter behandles med lægemidlet som en del af et klinisk forsøg.
SimpleImages / Getty Images
Hvad er multipelt myelom?
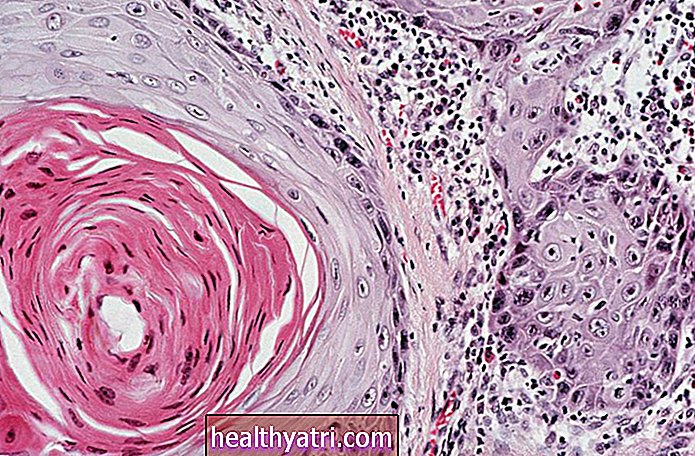
Multipelt myelom er en type sjælden, uhelbredelig kræft i blodet, også kendt som hæmatologisk kræft. Det påvirker celler kaldet plasmaceller, som er typer af hvide blodlegemer. Der er ingen kur mod multipelt myelom, og det vender næsten altid tilbage, på hvilket tidspunkt man siges at have en "tilbagefald eller ildfast" sygdom.
Hvordan fungerer Melflufen?
Da nye kombinationer af anti-myelom-lægemidler introduceres i tidligere behandlingslinjer, har mennesker med RRMM ofte sygdom, der er resistent over for flere lægemidler, og derfor er lægemidler med nye handlingsmekanismer presserende nødvendige.
Når Melflufen kombineres med steroiddexamethason, har det potentialet til at udfylde dette udækkede medicinske behov ved at give:
- En ny handlingsmekanisme
- Klinisk meningsfuld effektivitet
- Håndterbar sikkerhed
Melflufen dræber myelomaceller ved anvendelse af peptidaser (enzymer, der nedbryder peptider), som ofte findes i højere antal i myelomaceller end i raske celler. Når melflufen kommer ind i myelomaceller, bryder peptidaserne i cellen båndet, der holder melphalan og peptidasen sammen. Dette frigiver aktiv melphalan i myelomacellen. Melphalan forårsager derefter irreversibel DNA-skade, hvilket fører til celledød.
Hvad forskningen siger
Forskning er i gang for at finde nye behandlinger for myelomatose og finde ud af måder at forbedre brugen af eksisterende.
For at hjælpe med forskning kan du blive bedt om at deltage i et klinisk forsøg under din behandling.
Melflufen undersøges i øjeblikket som en behandling af RRMM-patienter i indstillinger for kliniske forsøg. De kliniske forsøg, der har undersøgt effekten af melflufen, inkluderer:
O-12-M1-undersøgelsen
O-12-M1 var et internationalt, multicenter, fase I / II-studie for at fastslå dosis af melflufen i kombination med dexamethason og undersøge behandlingsresponset hos patienter med RRMM, som var ildfaste (resistente) over for den sidste behandlingslinje. </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s>
I O-12-M1-studiet blev en gruppe på 45 patienter, der havde modtaget mindst to tidligere behandlinger, tilmeldt mellem juli 2013 og december 2016. Forsøget forsøgte at finde den maksimalt tolererede dosis melflufen. Den etablerede maksimale tolererede dosis var 40 mg melflufen i kombination med dexamethason.
Den testede kohort med den højeste dosis (55 mg) overskred den maksimalt tolererede dosis, fordi fire ud af seks patienter oplevede alvorlige bivirkninger, herunder neutropeni (lave hvide blodlegemer) og trombocytopeni (lavt antal blodplader); derfor blev den planlagte højeste dosis på 70 mg ikke testet.
For forsøgspatienterne førte behandling med melflufen og dexamethason til sygdomsstabilisering hos 76% af patienterne.
Mediantiden til næste behandling - start af behandlingen indtil næste behandling (eller til patientens død, alt efter hvad der skete først) - var 7,9 måneder. Patienterne levede i en median på 20,7 måneder.
HORIZON klinisk forsøg
I fase II HORIZON kliniske forsøg - som fandt sted på 20 steder i hele USA og Europa - blev melflufen og dexamethason givet til i alt 154 patienter, som i gennemsnit havde modtaget fem tidligere behandlingslinjer.
Alle patienter var tidligere blevet behandlet med et immunmodulatorisk lægemiddel og proteasomhæmmer, og de var resistente over for pomalidomid og / eller daratumumab.
Cirka tre ud af 10 patienter (29%) svarede på behandlingen, og den gennemsnitlige tid før myelom begyndte at komme tilbage var fire måneder. Disse resultater viste, at melflufen kan være gavnligt for patienter, der tidligere har haft flere behandlingslinjer.
Bivirkninger (AE'er) førte til dosisreduktion af melflufen hos 27% af patienterne og dosisforsinkelser hos 61% af patienterne. Den mest almindelige AE, der førte til dosisreduktion, var trombocytopeni (lavt antal blodplader), som forekom hos 14% af patienterne.
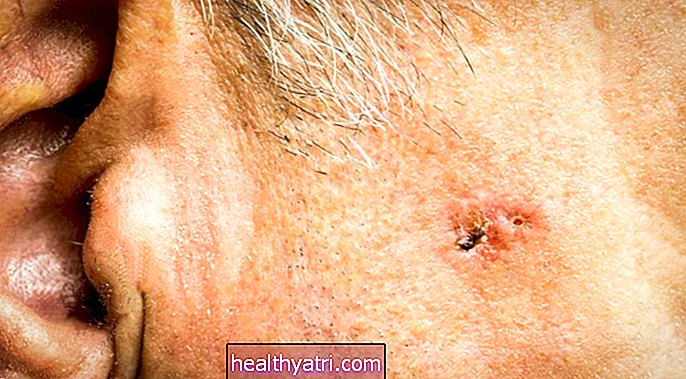
Alvorlige bivirkninger forekom hos 49% af patienterne generelt; hyppigst rapporteret var lungebetændelse (9%) og neutropeni (5%). Anden primær malignitet forekom hos fem patienter; af disse havde fire maligniteter med kutane manifestationer. Samlet set døde 10 patienter (6%) af behandlingsrelaterede bivirkninger.
Dosering
Melflufen gives ved intravenøs infusion (i venen). I kliniske forsøg har dosen været:
- 40 mg melflufen på den første dag i hver behandlingscyklus
40 mg dexamethason (reduceret dosis til patienter 75 år eller ældre) på dag 1, 8, 15 og 22 i hver 28-dages cyklus
I nogle forsøg blev dosis reduceret hos dem, der oplevede en bivirkning.
Bivirkninger
De mest almindeligt observerede bivirkninger af melflufen inkluderer:
• Lavt antal blodlegemer - neutropeni og trombocytopeni
• Anæmi
• Træthed
• Infektioner, herunder lungebetændelse og øvre luftvejsinfektioner
• Kvalme og diarré
Fordi melflufen er et relativt nyt lægemiddel, kan der opstå nye bivirkninger, der endnu ikke er rapporteret.
Risici
Da forskning er i gang, er det svært at vurdere risikoen ved at tage melflufen til RRMM. Da patienter, der er rekrutteret til kliniske forsøg, ofte har udtømt tidligere behandlinger, er chancerne for bivirkninger eller endog død under og efter behandlingen mulig.
Infektioner er en væsentlig årsag til sygelighed og dødelighed hos patienter med RRMM på grund af et forarmet immunsystem. Det er vigtigt regelmæssigt at overvåge dig selv for tegn på infektion og rapportere eventuelle bekymringer til din læge så hurtigt som muligt.
-lowers-risk-of-invasive-breast-cancer.jpg)



.jpg)





-diagnosed.jpg)


-is-diagnosed.jpg)










