Janus kinase (JAK) -hæmmere er en gruppe medikamenter, der hæmmer aktivitet og respons fra et eller flere af Janus kinase-enzymerne (JAK1, JAK2, JAK3 og TYK2). Disse enzymer fremmer normalt inflammation og autoimmunitet. Ved at interferere med enzymsignalveje kan JAK-hæmmere bruges til at hjælpe med at behandle kræft og inflammatoriske sygdomme, såsom reumatoid arthritis (RA) og psoriasisartritis (PsA).
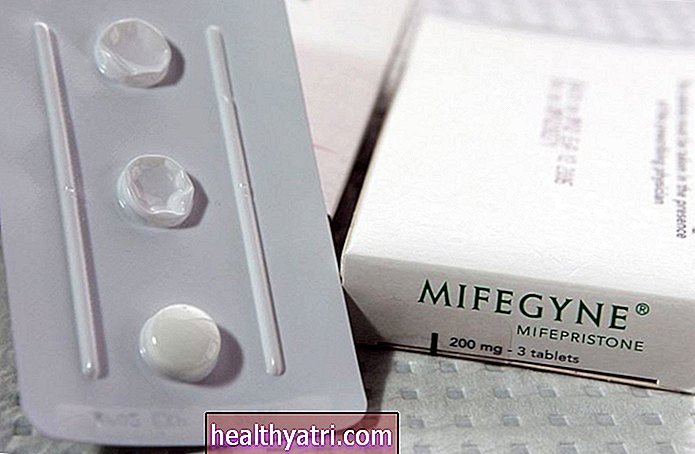
JAK-hæmmere kommer i pilleform, hvilket typisk er mere tiltalende end at skulle få en injektion eller infusion til et biologisk lægemiddel.
Jiaqi Zhou / VerywellKun en håndfuld JAK-hæmmerlægemidler er i øjeblikket tilgængelige i USA.
De er:
- Xeljanz (tofacitinib)
- Olumiant (baricitinib)
- Jakafi (ruxolitinib)
- Rinvoq (upadacitinib)
Alle de godkendte JAK-hæmmere er målrettet mod alle JAK-enzymerne. Flere andre, der i øjeblikket er under udvikling, er selektive for visse JAK-enzymer.
Hvad de gør
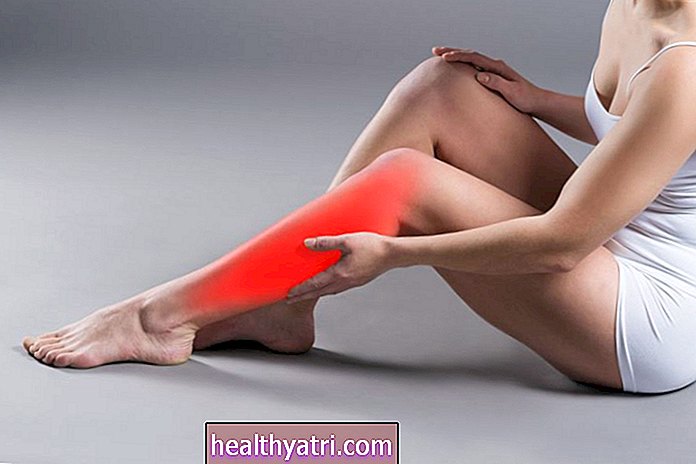
Overdreven betændelse kan være et problem under tilstande som RA, kræft og andre inflammatoriske tilstande.
Cytokiner er inflammatoriske proteiner, der binder til receptorer på immunceller. Dette signaliserer JAK-enzymer for at tilføje kemisk fosfat til deres receptorer, hvilket tiltrækker signaltransducer og aktivator for transkriptionsproteiner (STAT). STAT-proteinerne øger betændelsen yderligere.
Overaktivitet ved denne proces kan gøre dig modtagelig for alle former for autoimmune sygdomme - tilstande, hvor dit immunsystem angriber sunde, normale væv i din krop.
JAK-enzymer er vigtige bidragydere til processen, der skaber og opretholder autoimmunitet. Ved at blokere disse enzymer hæmmer JAK-hæmmere den autoimmune proces og mindsker effekten af de meddelelser, der kommer fra cytokiner. Dette beroliger et misfiring immunsystem, hjælper med at lette betændelse og lindrer andre relaterede symptomer.
Xeljanz (tofacitinib)
Xeljanz fik godkendelse fra U.S. Food and Drug Administration (FDA) i 2012 og er et af de mest ordinerede lægemidler i sin klasse.
Anvendelser
Xeljanx er godkendt til behandling af:
- Rheumatoid arthritis
- Psoriasisartritis
- Ulcerøs colitis
Selvom det i øjeblikket ikke er godkendt til andre anvendelser, har flere undersøgelser antydet, at Xeljanz kan være effektiv til behandling:
- Crohns sygdom
- Alopecia areata
- Vitiligo
- Psoriasis
- Atopisk dermatitis
Lægemidlet kan bruges off-label under disse og andre tilstande.
Formuleringer og dosering
Lægemidlet fås i en 5 mg (mg) pille og en 11 mg tablet med forlænget frigivelse.
Løbende forskning
Forskning omkring virkningen af Xeljanx på psoriasis har givet positive resultater.
En analyse i 2019 iBritish Journal of Dermatologysamlede data fra en fase 2-undersøgelse, fire fase 3-undersøgelser og en langvarig forlængelsesundersøgelse bestående af psoriasispatienter, der bruger tofacitinib. Forskere fandt ud af, at de, der bruger tofacitinib, oplevede en reduktion af symptomerne, herunder hudplaques, hvilket førte til forbedret livskvalitet.
Lægemidlet blev veltolereret, og sikkerhed og bivirkninger svarede til dem ved sygdomsmodificerende anti-reumatiske lægemidler (DMARD) behandlinger. Yderligere viste deltagere, der tog 10 mg dagligt, større forbedring end dem, der tog 5 mg dagligt.
Lægemidlets effektivitet var sammenlignelig med methotrexat eller det biologiske Enbrel (etanercept) i en dosis på 50 om ugen. Den højere dosis var sammenlignelig med en Enbrel-dosis på 100 mg pr. Uge.
Forfatterne konkluderede, at Xeljanz har en fordel-risikoprofil svarende til andre systemiske behandlinger og er en bedre mulighed for folk, der foretrækker oral terapi frem for injicerbare biologer.
Xeljanz for reumatoid arthritisForskning offentliggjort i januar 2019-udgaven afLancetantyder, at JAK-hæmmere er den sikreste og mest effektive behandling af alopecia areata, en autoimmun tilstand, der får hår til at falde ud i pletter. Lægemidlet antages at blokere nøglesignalveje, der er ansvarlige for sygdomsaktivitet.
Olumiant (baricitinib)
FDA godkendte Olumiant i 2018.
Anvendelser
Olumiant er godkendt til voksne med moderat til svær aktiv reumatoid arthritis, som ikke tidligere havde et tilstrækkeligt svar på behandlinger med methotrexat- eller tumornekrosefaktor (TNF) -hæmmere.
Det var blevet godkendt i Europa som andenlinjebehandling for moderat til svær RA hos voksne, enten som monoterapi (enkeltbehandling) eller i kombination med methotrexat.
Mens det ikke var godkendt til denne anvendelse på dette tidspunkt, foreslog en undersøgelse fra 2020, at kombination af baricitinib med direktevirkende antivirale stoffer kunne reducere infektivitet, viral replikation og inflammation forbundet med COVID-19.
Baricitinib er også blevet undersøgt som en psoriasisbehandling. En 2016-undersøgelse rapporterede signifikant forbedring af symptomerne, men der er behov for mere forskning. Brug til psoriasis betragtes som off-label.
Formuleringer og dosering
Olumiant fås som en 2 mg tablet taget en gang dagligt. FDA godkendte ikke dosis på 4 mg med henvisning til alvorlige bivirkninger. Undersøgelser havde vist, at øvre luftvejsinfektioner og høje kolesterolniveauer var sjældne, men hyppigere med baricitinib ved højere doser. </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s>
Løbende forskning
Ifølge en rapport fra 2019 offentliggjort iArthritis & Care Research,Olumiant monoterapi på 4 mg pr. Dag giver effektiv sygdomsbekæmpelse hos mennesker med leddegigt.
Patienterne i undersøgelsen, der ikke reagerede godt på baricitinib alene, viste forbedret sygdomskontrol, når methotrexat blev tilsat.
Jakafi (ruxolitinib)
Jakafi blev først godkendt af FDA i 2011.
Anvendelser
Jakifi er godkendt til behandling af:
- Mellemliggende eller højrisiko myelofibrose, herunder primær myelofibrose
- Post-polycytæmi vera myelofibrose
- Post-essentiel trombrocytæmi myelofibrose
Ruxolitinib kan bruges off-label til flere andre indikationer.
Det undersøges som en potentiel behandling for graft-versus-host-sygdom. Indtil videre har resultater været lovende hos mennesker med denne sygdom, der ikke har svær diarré, eller som ikke reagerede godt på andre tilgængelige terapier. </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s>
Det undersøges også for:
- Plaque psoriasis
- Alopecia areata
- Tilbagefald diffust stort B-celle lymfom
- Perifert T-celle lymfom
Formuleringer og dosering
Dette lægemiddel er tilgængeligt i tabletform i doser, der spænder fra 5 mg til 25 mg. Blodpladeantallet skal overvåges, før Jakafi startes, og mens det tages på grund af en risiko for trombocytopeni, anæmi og neutropeni.
Løbende forskning
Ruxolitinib (INCB18424) blev udviklet til behandling af mellemliggende eller højrisiko myelofibrose, der påvirker knoglemarv, og til polycytæmi vera, når andre behandlinger har mislykkedes. Det er designet til at hæmme JAK1 og JAK2. Fase 3-undersøgelser har vist betydelige fordele ved lindring af myelofibrose-symptomer.
I slutningen af 2011 blev topisk Ruxolitinib godkendt til behandling af myelofibrose. Det blev godkendt i 2014 til behandling af polycythemia vera.
Ruxolitinib kliniske forsøg er i øjeblikket i gang til behandling af plaque psoriasis, alopecia areata, kræft i bugspytkirtlen og to typer lymfom.
Rinvoq (upadacitinib)
Rinvoq er et nyere lægemiddel i denne gruppe, der har fået FDA-godkendelse i 2019.
Anvendelser
Rinvoq er godkendt til behandling af voksne med moderat til svær aktiv reumatoid arthritis, der ikke reagerede godt eller ikke kunne tåle methotrexat.
Undersøgelser pågår for Rinvoq som en behandling af:
- Crohns sygdom
- Ulcerøs colitis
- Atopisk dermatitis
- Ankyloserende spondylitis
- Psoriasis
- Psoriasisartritis
- Inflammatorisk tarmsygdom
Disse anvendelser er ikke godkendt af FDA og betragtes derfor som off-label.
Formuleringer og dosering
Dette lægemiddel er tilgængeligt i en 15 mg tabletform, der skal tages en gang dagligt.
Løbende forskning
Resultaterne har generelt været positive for Rinvoq som en behandling til de ikke-godkendte anvendelser, der er anført ovenfor.
Forskning offentliggjort i slutningen af 2019 rapporterede, at upadacitinib var effektiv og veltolereret hos mennesker med aktiv ankyloserende spondylitis, som ikke tolererede eller reagerede godt på ikke-steroide antiinflammatoriske lægemidler (NSAID'er). Forfatterne anbefalede yderligere undersøgelse af lægemidlet til axiale sponyloarthritis-typer.
Hvad er der i rørledningen?
Pipeline-lægemidler udvikles i øjeblikket og testes, men er endnu ikke FDA-godkendt til brug. Hvert af disse lægemidler skal gennemgå tre faser af kliniske forsøg, før det kan bringes til FDA til godkendelse.
Flere JAK-hæmmere finder vej gennem rørledningen og gennemgår kliniske forsøg, der sigter mod at bestemme deres sikkerhed og effektivitet ved behandling af en række autoimmune tilstande.
Filgotinib (GLPG0634)
Filgotinib er en meget selektiv JAK1-hæmmer, der testes som en behandling for:
- Rheumatoid arthritis
- Psoriasisartritis
- Inflammatorisk tarmsygdom (Crohns sygdom, colitis ulcerosa)
- HIV-sygdom
"Meget selektiv" betyder, at det kun er målrettet mod bestemte JAK-enzymer snarere end en stor gruppe af dem. Forskere antager, at dette kan betyde højere doser med færre bivirkninger.
Status
Fase 3-forsøg er afsluttet. I slutningen af 2019 indsendte producenten en ny lægemiddelansøgning (NDA) sammen med en ansøgning om prioriteret gennemgang, som undertiden fremskynder godkendelsesprocessen.
I august 2020 afviste FDA stoffet på grund af toksicitet. Ansøgninger er også indsendt til tilsynsmyndigheder i Europa og Japan.
Forskning Højdepunkter
Her er et udsnit af takeaways fra forskning i filgotinib hidtil.
Brug til RA:
- To fase 2b-forsøg med RA har vist, at dette lægemiddel er effektivt både i kombination med methotrexat og som monoterapi.
- Fase 3-forsøg har vist, at filgotinib er effektivt for mennesker med aktiv RA, som ikke reagerede på eller ikke kunne tåle biologiske DMARDs, og for dem, der aldrig har taget methotrexat.
- Et års lang fase 3-forsøg viste, at resultaterne var konsistente for undersøgelsens fulde varighed.
- En analyse, der sammenlignede filgotinib ved forskellige doser og i kombination med forskellige RA-lægemidler, viste, at en daglig dosis på enten 100 mg eller 200 mg plus methotrexat var det mest effektive behandlingsregime for RA. Forfatterne rapporterer ingen signifikant risiko for alvorlige bivirkninger.
Anvendelse til andre sygdomme:
- For psoriasisgigt viste et fase 2-forsøg i 2020, at filgotinib signifikant forbedrede sundhedsrelateret livskvalitet hos 131 deltagere.
- For Crohns sygdom viste en fase 2-undersøgelse fra 2017, at filgotinib førte til remission af symptomer markant mere end placebo hos mennesker med aktiv sygdom.
- Ifølge en anden 2020-undersøgelse ser filgotinib ud til at foretage gavnlige ændringer, der kan reducere immunsystemaktivering i HIV-sygdom.
Peficitinib (ASP015K)
Peficitinib hæmmer to specifikke enzymer, JAK 1 og JAK 3, og undersøges i øjeblikket til behandling af reumatoid arthritis.
Status
Fase 3-forsøg er afsluttet, og producenten har indsendt en ny lægemiddelansøgning til FDA. Dette lægemiddel er godkendt til behandling af reumatoid arthritis i Japan under varemærket Smyraf.
Forskning Højdepunkter
- Lægemidlet har vist sig at forbedre RA-resultaterne i to fase-2b-undersøgelser.
- To fase 3-forsøg har vist, at peficitinib kan forbedre resultaterne hos mennesker med RA, som ikke reagerede godt på andre lægemidler og har moderat til svær aktiv sygdom.
- Undersøgelser tyder på, at peficitinib er bedre end placebo til at reducere symptomer og undertrykke ledskader.
- Det var veltolereret og havde positive resultater, der forblev konsistente i hele et års undersøgelse.
Itacitinib (INCB039110)
Itacitinib undersøges som en behandling for:
- Plaque psoriasis
- Kronisk transplantat-mod-vært sygdom
Det er også blevet foreslået som en mulig behandling for COVID-19 på grund af specifikke virkninger, det har på immunsystemet.
Status
Fase 2-forsøg er i øjeblikket i gang for at teste effektiviteten og sikkerheden af Itacitinib til behandling af plaque psoriasis. Lægemidlet er gået videre til fase 3 for kronisk graft-versus-host-sygdom på trods af, at de ikke har forsøgt at undersøge den akutte form af tilstanden.
Fra midten af 2020 var forskningen endnu ikke påbegyndt for COVID-19.
Forskning Highlight
En fase 2-undersøgelse offentliggjort i 2016 demonstrerede signifikant forbedring i en vurdering af plaque psoriasis-symptomer.
Abrocitinib (PF-04965842)
Abrocitinib er en oral selektiv JAK1-hæmmer, der i øjeblikket undersøges til behandling af:
- Plaque psoriasis
- Atopisk dermatitis, moderat til svær, hos voksne og unge
- Vitiligo
- Alopecia Areata
- Autoimmune sygdomme med JAK1-involvering
Status
Dette lægemiddel er endnu ikke godkendt til brug. I juni 2020 begyndte fase 2, fase 2b og fase 3 kliniske forsøg med abrocitinib som behandling for atopisk dermatitis. Mindst et fase 2-forsøg med plaque psoriasis er afsluttet. Andre potentielle anvendelser er i tidligere stadier af undersøgelsen.
Forskning Højdepunkter
- Abrocitinib har gennemført mindst en fase 2-undersøgelse, det demonstrerede, at det forbedrede symptomerne og var veltolereret.
- Forskning fra en undersøgelse fra British Association of Dermatologists fra 2017 viser, at abrocitinib var veltolereret og effektiv til forbedring af symptomer på moderat til svær plaque psoriasis.
- En undersøgelse fra 2018 foreslog, at stoffet generelt kunne være gavnligt ved inflammatoriske sygdomme. En anden artikel fra det år citerer beviser fra dyreforsøg, der tyder på, at abrocitinib undersøges for autoimmune sygdomme.
SHR0302
SHR0302 menes at være en meget selektiv JAK1-, JAK2- og JAK3-inhibitor. Det undersøges som en mulig behandling for:
- Rheumatoid arthritis
- Ankyloserende spondylitis
- Lupus
- Crohns sygdom
- Ulcerøs colitis
- Alopecia areata
- Atopisk dermatitis
- Myoproliferative svulster (en type blodkræft)
- Leverfibrose (en leversygdom)
Status
Dette lægemiddel er endnu ikke godkendt til brug. I maj 2020 iværksatte forskere i USA og Kina fase 2 kliniske forsøg med alopecia areata, og kinesiske forskere indledte et fase 1-forsøg på leverinsufficiens. I juni 2020 startede fase 2 og 3 forsøg med ankyloserende spondylitis.
I 2019 startede kliniske fase 2-forsøg med ulcerøs colitis og Crohns sygdom. Lægemidlet har også nået fase 2-forsøg med atopisk dermatitis. Fase 3-forsøg med reumatoid arthritis forventes afsluttet i 2022. Foreløbig forskning er begyndt for lupus.
Forskning Højdepunkter
Indtil videre er meget lidt forskning på dette lægemiddel afsluttet og offentliggjort.
- En 2019-undersøgelse fra Kina foreslog, at SHR0302 kan hæmme væksten af myoproliferative neoplasmer og nedsætte inflammation ved at ændre JAK-STAT-signalvejen. Imidlertid var disse effekter svagere end Jakafis.
- En 2016-undersøgelse viste, at SHR0302 kan lindre hepatisk fibrose ved at målrette mod funktioner i leverstellatceller.
- En 2016-undersøgelse viste, at lægemidlet foretog adskillige potentielt gavnlige ændringer i immunfunktionen hos rotter med lægemiddelinduceret arthritis.
BMS-986165
BMS-986165 undersøges i øjeblikket til behandling af:
- Plaque psoriasis (moderat til svær)
- Crohns sygdom
- Ulcerøs colitis
- Psoriasisartritis
- Lupus
- Autoimmun sygdom
Status
Fra midten af 2020 var dette lægemiddel i fase 3-forsøg med plaque psoriasis; fase 2-forsøg med Crohns sygdom, psoriasisgigt, lupus og colitis ulcerosa; og fase 1-forsøg for autoimmune sygdomme generelt.
Forskning Højdepunkter
- Data fra fase II-undersøgelser viser, at lægemidlet var effektivt til at lindre symptomer hos mennesker med plaque psoriasis, der tog 3 mg eller mindre om dagen i en periode på 12 uger.
- En undersøgelse fra 2019 siger, at BMS-986165 er unik blandt JAK-hæmmere og kan have egenskaber, der gør den særlig effektiv mod autoimmune sygdomme.
Hvorfor har rørledningslægemidler kodelignende navne?
I de tidligste stadier får et nyt lægemiddel et alfanumerisk navn. Senere er det tildelt et generisk navn. Når det er godkendt af FDA, giver producenten det et mærke. Typisk er lægemiddelnavne skrevet med mærkenavnet først og det generiske navn i parentes.
Mulige bivirkninger
Alle stoffer har mulige bivirkninger. Hver JAK-hæmmer har sin egen unikke liste over potentielle bivirkninger.
Der er dog nogle, der deles blandt dem. Nogle almindelige kan forsvinde, når din krop er vant til medicinen. Andre kan vedblive og have mere alvorlige virkninger.
almindelige
Almindelige bivirkninger, der kan forsvinde ved brug, inkluderer:
- Diarré
- Hovedpine
- Forkølelsessymptomer, såsom ondt i halsen eller en løbende eller tilstoppet næse
- Svimmelhed
- Let blå mærker
- Vægtøgning
- Oppustethed og gas
- Træthed
Åndenød og andre alvorlige og igangværende bivirkninger skal rapporteres til din læge. Nogle kan styres gennem livsstil og medicin, mens andre kræver en medicinskift.
Immunsystemsundertrykkelse
I lighed med biologiske stoffer og traditionelle DMARD'er undertrykker JAK-hæmmere immunsystemet. Selvom det er det, der gør dem gavnlige, betyder det, at de også kan øge sårbarheden over for alvorlige infektioner - især infektioner i øvre luftveje og urinveje.
I kliniske undersøgelser er nogle mennesker kommet med tuberkulose (TB), en meget alvorlig bakteriel lungeinfektion. Folk, der tager JAK-hæmmere, har også en øget risiko for helvedesild, en virusinfektion, der forårsager et smertefuldt udslæt.
Hvis du holder op med at bruge disse stoffer på grund af infektion (er), skal dit immunsystem vende tilbage til det normale og begynde at forhindre infektioner igen.
Nogle mennesker kan have en øget risiko for kræft, fordi lægemidler til JAK-hæmmer blokerer de immunprocesser, der er ansvarlige for forebyggelse af tumorer.
Andet
JAK-hæmmere kan også forårsage anæmi (lavt antal røde blodlegemer) hos nogle mennesker. Dette skyldes den måde, de påvirker proteiner på, som kroppen har brug for for at fremstille røde blodlegemer.
JAK-hæmmere er også kendt for at sænke antallet af hvide blodlegemer, en tilstand kaldet lymfopeni.
Disse lægemidler kan også påvirke kolesteroltal. Din læge skal muligvis ordinere et statinlægemiddel, såsom Lipitor (atorvastatin), for at regulere dit kolesterol.
Blodpropper kan forekomme, hvilket resulterer i en øget risiko for kardiovaskulære hændelser, dyb venetrombose og lungeemboli.
Leverskader er også en mulig bivirkning ved brug af JAK-hæmmer. Og disse lægemidler er kontraindiceret hos patienter med diverticulitis, da de kan føre til tyktflydende perforering.
Et ord fra Verywell
Hvis du har en autoimmun tilstand og har det godt med ældre lægemidler (såsom biologiske stoffer eller methotrexat), har du sandsynligvis ikke brug for en JAK-hæmmer. Men hvis du ikke har haft succes med de ældre behandlinger, kan en JAK-hæmmer muligvis tilbyde nødvendig lindring.
Disse medikamenter er dog ret nye, og forskere lærer bare om deres langsigtede sikkerhed.Du kan tale med din læge for at se, om du kan tage dem sammen med andre lægemidler og kosttilskud (interaktioner er mulige) og rapportere om aktuelle eller igangværende bivirkninger.
Hvad er der i rørledningen til RA-behandling?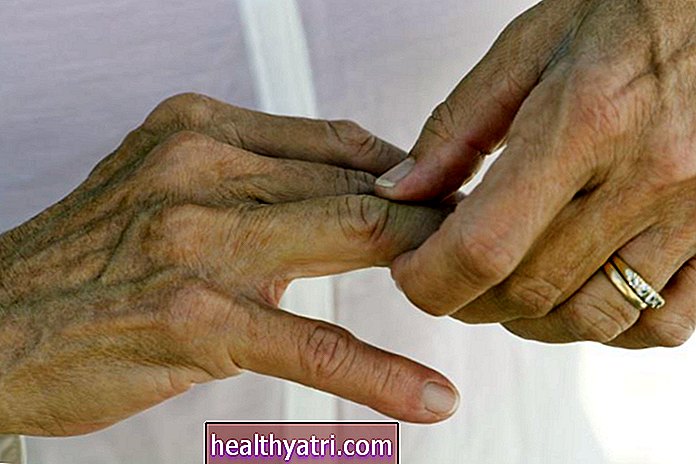



.jpg)


.jpg)