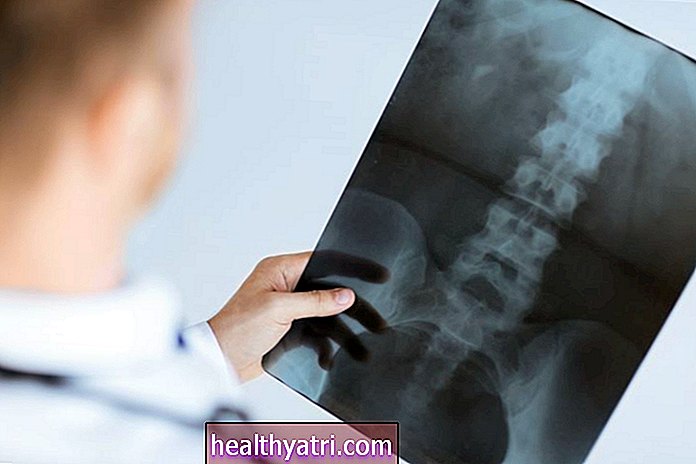
Hæmoglobinelektroforese er en blodprøve, der almindeligvis bruges til at diagnosticere og karakterisere hæmoglobinlidelser, kaldet hæmoglobinopatier. Hæmoglobin er et komplekst protein indeholdt i de røde blodlegemer, hvis opgave er at bære og levere ilt gennem kroppen. Hæmoglobin henter ilt fra lungerne, transporterer ilt gennem blodbanen og frigiver det på det rigtige tidspunkt, så det kan bruges af alle kroppens væv. Der er flere nedarvede hæmoglobinopatier, der kan påvirke hæmoglobins evne til at udføre sit job normalt.
Formålet med testen
Hæmoglobin-elektroforesetesten er designet til at detektere genetiske abnormiteter i strukturen af en persons hæmoglobin. Hæmoglobinelektroforese udføres typisk, når en person har tegn eller symptomer på hæmolytisk anæmi, en familiehistorie af en hæmoglobinopati, en unormal komplet blodtællingstest (CBC) eller en positiv neonatal screeningstest.
I øjeblikket anbefaler American College of Obstetricians and Gynecologists i USA screening for hæmoglobinopati for alle gravide kvinder ved at udføre CBC-test efterfulgt af en hæmoglobin-elektroforese, hvis CBC er unormal; eller hvis kvinden har højere risiko for en hæmoglobinopati baseret på etnicitet. Kvinder af afrikansk, middelhavs, sydøstasiatisk, vestindisk eller mellemøstlig herkomst har højere risiko for hæmoglobinopatier. De mandlige partnere for kvinder, der viser sig at have hæmoglobinopatier, bør også have screening, hvis de overvejer at få et barn.
Verywell / JR BeeHæmoglobinelektroforesetesten er en blodprøve, der kan påvise normale og unormale hæmoglobiner og begynde at karakterisere typen af hæmoglobinopati, hvis der findes nogen. Hæmoglobinelektroforese er dog kun en af flere tests, der kan opdage og karakterisere unormale hæmoglobiner. Ofte, hvis der opnås et unormalt resultat med elektroforesetesten, kan der foretages sofistikeret test for mere præcist at karakterisere hæmoglobinopatier.
Hæmoglobinelektroforese udføres ved at placere en lille mængde blod på specielt papir eller en speciel gel og udsætte den for en elektrisk strøm. Forskellige globiner har forskellige elektriske ladninger og kan differentieres fra hinanden baseret på deres adfærd, når de udsættes for en elektrisk strøm. Forskellige typer globin bevæger sig på tværs af papiret (eller gelen) ved forskellige hastigheder og adskiller sig således i karakteristiske bånd. Ved at undersøge de bånd, der dannes under anvendelsen af strømmen, kan de typer hæmoglobin, der er til stede i blodprøven, differentieres.
Risici og kontraindikationer
Hæmoglobin-elektroforesetesten er en blodprøve. Derfor er der næsten ingen risiko bortset fra den lille risiko for blå mærker, blødning eller infektion, der er til stede ved enhver test, der kræver blodtrækning.
Generelt er det bedst ikke at have testet hæmoglobinelektroforese inden for 12 uger efter en blodtransfusion, fordi det er muligt at forveksle resultater af hæmoglobiner fra de transfunderede røde blodlegemer.
Før testen
Hæmoglobintypen i dit blod er ikke relateret til tidspunktet på dagen eller hvad du har spist eller drukket for nylig, så der er ingen specielle instruktioner eller begrænsninger, du bliver nødt til at følge, før du får en hæmoglobinelektroforese. Prøven kan tages på ethvert anlæg, der udfører standardblodtrækning, når som helst på dagen. Det gøres typisk på et lægekontor, et laboratorium eller et hospital. Som med enhver blodprøve skal du bære behageligt tøj med løse ærmer, der let kan trækkes op for at udsætte din arm.
Hæmoglobin-elektroforesetesten er normalt dækket af sundhedsforsikring, så længe lægen giver forsikringsselskabet en rimelig forklaring på, hvorfor testen er angivet. Det er dog altid bedst at tjekke med dit forsikringsselskab, før du tager testen, bare for at sikre dig. Du skal medbringe dit forsikringskort, når du har udført blodprøven.
Under testen
Hæmoglobin-elektroforesetesten udføres med en standardblodtrækning. En turnet placeres på din arm, og en tekniker vil føle en passende vene. Din hud rengøres med en spritserviet, og en nål indsættes i venen og blodprøven tages. Når blod er trukket, påføres der en lille bandage eller gasbind. Du får derefter lov til at gå hjem.
Efter testen
Komplikationer fra et blodtræk er ekstremt usædvanligt. Hold øje med yderligere blødninger, blå mærker eller betændelse eller infektion. Hvis der skulle opstå blødning, skal du lægge mere pres på punkteringsstedet i 5 til 10 minutter, og hvis problemet fortsætter, skal du kontakte din læge. Du bør også ringe til din læge, hvis du ser tegn på betændelse eller infektion (rødme, ømhed, overdreven smerte eller hævelse).
Fortolkning af resultater
Du kan forvente at høre resultaterne af din hæmoglobin-elektroforesetest inden for få dage til en uge. Hvis din test er normal, kan det være, at det er alt, hvad du vil høre.
Du kan dog få en mere detaljeret rapport - eller du kan bede om en detaljeret rapport - selvom testen er normal.
Normale hæmoglobinværdier
Hos voksne er normale værdier for hæmoglobinmolekyler angivet i procent som følger:
- Hæmoglobin A: 95% –98%
- Hæmoglobin A2: 2% –3%
- Hæmoglobin F: 0,8% -2%
- Hæmoglobiner S, C, D, E og andre: 0%
Hos børn er højere niveauer af hæmoglobin F typiske med tilsvarende lavere niveauer af hæmoglobin A og A2:
- Hæmoglobin F hos nyfødte: 50% –80%
- Hæmoglobin F op til 6 måneder: 8%
- Hæmoglobin F over 6 måneder: 1% -2%
Unormale resultater
Hvis du har en mængde unormalt hæmoglobin på din hæmoglobinelektroforese, har du brug for yderligere evaluering.
Din læge bliver nødt til at tage højde for mange yderligere faktorer, når du fortolker betydningen af det unormale hæmoglobin, herunder din familiehistorie, resultaterne af din CBC (herunder især hæmoglobin, hæmatokrit og det gennemsnitlige kropuskulære volumen), udseendet af din røde blodlegemer under mikroskopet og resultaterne af dine serumjernundersøgelser.
Derudover kan din læge muligvis anvende mere sofistikerede teknikker til fuldt ud at karakterisere og kvantificere det unormale hæmoglobin i dine blodprøver. Sådan test kan omfatte højtryksvæskekromatografi, kapillærzoneelektroforese, isoelektrisk fokusering eller målrettet genetisk testning.
Forståelse af hæmoglobin og hæmoglobinopatier
Hvert hæmoglobinmolekyle er en kompleks struktur bestående af fire proteinunderenheder kaldet globiner, som hver er bundet til en ikke-protein, jernholdig struktur kaldet en hæmgruppe. De fire globinenheder i et hæmoglobinmolekyle består af to alfa-lignende og to beta-lignende kæder.
Hver globinenhed bærer en hæmgruppe bestående af en porphyrinring og en jernion. Det er hæmgruppens opgave at binde og transportere ilt og frigive det til det perifere væv på det rigtige tidspunkt. Hvert hæmoglobinmolekyle kan binde fire iltmolekyler.
Hæmoglobins evne til at binde til ilt - der kaldes hæmoglobins iltaffinitet - bestemmes i vid udstrækning af globinunderenhederne i hæmoglobinkomplekset. Baseret på lokale miljøfaktorer (især blodets surhedsgrad og den lokale iltkoncentration) ændrer globin-underenhederne deres form efter behov for at ændre affiniteten af deres respektive hæmgrupper til ilt. Denne kalibrerede iltaffinitet af hæmoglobin gør det muligt at samle iltmolekyler og derefter frigive dem på de rigtige tidspunkter.
Når blod cirkulerer gennem lungerne, diffunderer ilt ind i de røde blodlegemer. I det lokale miljø i lungerne optages iltet og bindes af hæmoglobinmolekyler. Det iltbærende hæmoglobin udføres derefter til vævene. Da hæmoglobinet udsættes for et stadig mere surt miljø i det perifere væv (forårsaget af kuldioxidaffald produceret af cellemetabolisme) mister det noget af dets affinitet for ilt. Oxygenet frigives således til vævene.
Det nyligt deoxygenerede hæmoglobin i det perifere væv samler noget af det overskydende kuldioxid, det finder der, og fører det tilbage til lungerne. (Det meste af affaldet kuldioxid når dog lungerne, efter at det er opløst i blodet.)
Hæmoglobin tegner sig for blodets farve. Hæmoglobin i arterierne, der bærer masser af ilt, har en lys rød farve (det er sådan, at røde blodlegemer fik deres navn). Hæmoglobin i venerne, der har leveret sit ilt til vævene, bliver mere blålig i farven.
Typer af normalt hæmoglobin
Der er flere typer hæmoglobin, som er kendetegnet ved de specifikke typer globiner, de indeholder. Normalt voksent hæmoglobin består af to alfa- og to beta-globiner. Andre typer hæmoglobiner indeholder lignende globiner, ofte omtalt som alfa-lignende og beta-lignende globiner.
Tre forskellige slags hæmoglobin bæres normalt af røde blodlegemer i forskellige stadier af menneskelig udvikling. Disse tre normale hæmoglobiner er optimeret til deres miljø.
I meget tidlig drægtighed, når det menneskelige embryo modtager sit ilt fra æggeblommesækken, produceres embryonale hæmoglobiner. De unikke globinstrukturer af embryonalt hæmoglobin muliggør tilstrækkelig iltudveksling i det relativt lave iltmiljø i det tidlige føtalliv.
Efterhånden som fostercirkulationen udvikler sig, og der opnås ilt fra moderkagen (som giver højere iltkoncentrationer end æggeblommesækken, men stadig lavere end til sidst vil blive tilvejebragt af lungerne), vises en anden form for hæmoglobin, kaldet føtal hæmoglobin. Fosterhæmoglobin vedvarer i resten af drægtigheden og erstattes gradvist af voksen hæmoglobin i de første par måneder efter fødslen.
Endelig er voksenhæmoglobin, der er fremherskende seks måneder efter fødslen, optimeret til iltudveksling mellem lungerne med højt iltmiljø og det lave iltmiljø i det perifere væv.
Disse tre normale humane hæmoglobiner er kendetegnet ved forskellige globiner. Normal voksen hæmoglobin (kaldet hæmoglobin A) består af to alfa- og to beta-globiner. Hæmoglobin A2 består af to alfa- og to delta-globiner. Fosterhæmoglobin (hæmoglobin F) indeholder to alfa- og to gamma (beta-lignende) globiner. Der er forskellige typer embryonalt hæmoglobin, der indeholder flere kombinationer af alfa-, gamma-, zeta- og epsilon-globiner.
Hæmoglobinopatier
Talrige genetiske mutationer er blevet opdaget, der resulterer i abnormiteter af enten de alfa-lignende eller beta-lignende globiner i hæmoglobinmolekylet. De unormale hæmoglobiner som følge af disse mutationer kaldes hæmoglobinopatier.
Over 1.000 slags hæmoglobinopatier er hidtil blevet karakteriseret. De fleste af disse er af mindre betydning og ser ikke ud til at forårsage kliniske problemer. De er blevet opdaget, stort set tilfældigvis, hos tilsyneladende normale mennesker med fremkomsten af screening af hæmoglobinelektroforesetest.
Imidlertid producerer flere hæmoglobinopatier sygdom. Alvorligheden af en hæmoglobinopati afhænger normalt af, om mutationen er homozygot (arvet fra begge forældre) eller heterozygot (arvet fra kun den ene forælder med normale hæmoglobingener fra den anden forælder). Generelt produceres der med heterozygote hæmoglobinopatier tilstrækkeligt "normalt" hæmoglobin til i det mindste i nogen grad at afbøde de samlede kliniske manifestationer. Mennesker med homozygote former for hæmoglobinopati har tendens til at have en mere alvorlig klinisk sygdom.
Hæmoglobinopatierne er generelt opdelt i to kategorier:
- Hæmoglobinopatier, der manifesteres ved strukturelle eller funktionelle ændringer i hæmoglobinmolekylet. Disse kaldes generelt de strukturelle hæmoglobinopatier.
- Hæmoglobinopatier, der manifesteres ved reduceret produktion af en af globinkæderne. Hæmoglobinopatier i denne anden kategori kaldes thalassemier.
Strukturelle hæmoglobinopatier
Flere strukturelle hæmoglobinopatier er blevet identificeret, der producerer klinisk sygdom. Strukturelle ændringer i hæmoglobinmolekylet kan forårsage ændringer i formen og fleksibiliteten af de røde blodlegemer. De uformede røde blodlegemer kan forårsage okklusion af blodkar. Andre former for strukturelle hæmoglobinopatier kan forårsage hæmolytisk anæmi. Alligevel kan andre strukturelle abnormiteter ændre affiniteten af hæmoglobin til ilt. Hæmoglobinopatier med lav affinitet kan forårsage polycytæmi (for mange røde blodlegemer). Hæmoglobinopatier med høj affinitet kan forårsage cyanose (ilt-sult i vævene).
Almindelige strukturelle hæmoglobinopatier inkluderer:
- Hæmoglobin S (seglcelle) er forårsaget af en mutation i beta-globinkæden. Den homozygote form af seglcellesygdom kan forårsage okklusion af blodkar i perioder med stress (seglcellekrise), hvilket fører til smerte, infektioner, hævelse og endnu mere alvorlige konsekvenser såsom slagtilfælde. Den heterozygote form kaldes seglcelleegenskaber og forårsager normalt ikke kliniske problemer.
- Hæmoglobin C, hæmoglobin D og hæmoglobin E er alle forårsaget af mutationer i beta-globinkæden. De homozygote former for disse lidelser producerer hæmolytisk anæmi og miltforstørrelse. De heterozygote former producerer normalt ikke signifikant sygdom.
Reduceret hæmoglobinproduktion
Thalassemierne er hæmoglobinopatier, der er forårsaget af abnormiteter i de gener, der styrer produktionen af globiner. Dette medfører en reduceret produktion af en af globinkæderne, hvilket resulterer i reduceret produktion af hæmoglobin og dermed anæmi. Mennesker med thalassæmi kan også lide af jernoverbelastning og øget risiko for infektioner.
Alfa-thalassemier, som oftest ses hos mennesker af asiatisk eller afrikansk herkomst, resulterer i reduceret alfa-globinproduktion. Beta-thalassemier, der ofte ses hos mennesker af middelhavsafstamning, forårsager reduceret produktion af beta-globin.
Thalassemier er genetisk komplekse lidelser, da flere genetiske mutationer (alene eller i kombination) kan producere thalassæmi. Alvorligheden af thalassæmi afhænger af, hvilken globinkæde der er involveret, og hvor mange og hvilke specifikke gener der forårsager problemet.
Kombination af hæmoglobinopatier
Lejlighedsvis arver folk forskellige hæmoglobinopati-gener fra hver forælder, hvilket resulterer i det, der kaldes en sammensat heterozygot hæmoglobinopati eller en kombination af hæmoglobinopati. De mere almindelige kombination hæmoglobinopatier inkluderer:
- Hæmoglobin SC-sygdom, hvor hæmoglobin S kommer fra den ene forælder, og hæmoglobin C kommer fra den anden. Klinisk har mennesker med hæmoglobin SC tendens til at have en mildere form for seglcellesygdom, men manifestationer kan variere meget.
- Segl / beta-thalassæmi, hvor hæmoglobin S kommer fra den ene forælder, og beta-thalassæmi kommer fra den anden. Disse mennesker kan have typiske manifestationer af seglcelleanæmi og anæmi.
Opfølgning
Når hæmoglobinopati er blevet karakteriseret fuldt ud, bør du forvente, at din læge har en detaljeret diskussion med dig om to emner: behandling, du muligvis har brug for (og eventuelt), og genetisk rådgivning.
Hvis din hæmoglobinopati er den heterozygote form (såkaldt hæmoglobin "træk", hvor du kun har arvet det unormale hæmoglobin fra den ene forælder), vil mellem 45% og 65% af dit hæmoglobin sandsynligvis være normal voksen hæmoglobin, og dine symptomer , hvis nogen, sandsynligvis være milde. De fleste mennesker med hæmoglobinegenskaber kræver ikke nogen specifik behandling.
Hvis du har en homozygot hæmoglobinopati eller en kombination af hæmoglobinopati (det vil sige to forskellige unormale hæmoglobiner), kan du få brug for behandling.
Mennesker med seglcellesygdom i dag diagnosticeres næsten altid i barndommen med rutinemæssige screeningstests for hæmoglobin. Disse babyer behandles med antibiotikaprofylakse, vitamintilskud, fuld vaccination og aggressiv styring af en seglcellekrise, når den opstår.
Thalassemierne er en gruppe lidelser, hvis virkninger varierer meget afhængigt af den specifikke genetiske mutation, der forårsager dem. Det mest almindelige problem, de forårsager, er anæmi, men thalassæmi kan også forårsage abnormiteter i skelettet og overbelastning af jern såvel som væksthæmning og andre lidelser. Mennesker med svær thalassæmi kan kræve hyppige blodtransfusioner og splenektomi. Jernoverbelastning kan blive et stort problem hos mennesker med thalassæmi.
Flere usædvanlige hæmoglobinopatier fører til "ustabile hæmoglobiner", hvor strukturen af hæmoglobinmolekylerne ændres på en sådan måde at reducere levetiden for de røde blodlegemer. Mennesker med disse tilstande kan opleve anæmi, forstørrede milt og hyppige infektioner. Behandlingen sigter mod at forhindre komplikationer og kan omfatte blodtransfusioner, splenektomi og undgå oxidationsmedicin, herunder visse antibiotika og NSAID'er. Knoglemarvstransplantation anvendes også oftere til mennesker med svær, livstruende hæmoglobinopatier.
Genetisk rådgivning
Hvis risikoen for at producere en baby med alvorlig hæmoglobinopati vurderes at være forhøjet, kan føtal evaluering være indiceret, når graviditet opstår.







.jpg)





.jpg)