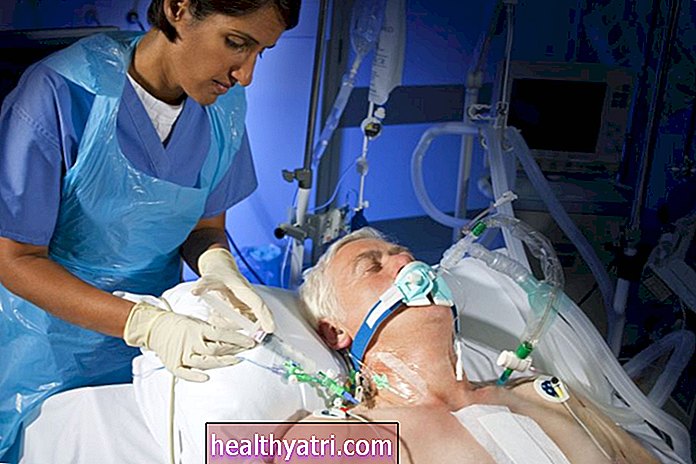
Dex Images / Getty Images
Vigtigste takeaways
- FDA har godkendt en kombination af bamlanivimab og etesevimab til behandling af COVID-19 hos patienter, der har høj risiko for at udvikle komplikationer.
- Den nye kombination "reducerede" signifikant risikoen for alvorlige komplikationer i et klinisk forsøg.
- FDA godkendte tidligere bamlanivimab alene til brug.
Food and Drug Administration (FDA) har godkendt en anden monoklonal antistofbehandling til behandling af patienter med COVID-19. Agenturet udstedte en nødbrugsgodkendelse (EUA) til lægemidlerne bamlanivimab og etesevimab, der blev brugt sammen til behandling af mild til moderat COVID-19 hos personer i alderen 12 år og derover, som har høj risiko for at udvikle svær COVID-19.
Et klinisk forsøg viste, at en enkelt IV-infusion af bamlanivimab og etesevimab "reducerede" signifikant risikoen for indlæggelse og død fra COVID-19 i løbet af 29 dages opfølgning sammenlignet med placebo hos patienter med virussen, som havde en høj risiko for udvikler sig til svær sygdom.
Forsøget omfattede 1.035 ikke-indlagte voksne med milde til moderate COVID-19 symptomer, som havde høj risiko for at udvikle sig til svær COVID-19 og enten gav dem en enkelt infusion af 2.800 mg bamlanivimab og etesevimab eller placebo. Forskere fandt ud af, at 36 patienter (7%), der fik placebo, var indlagt på hospitalet eller døde sammenlignet med 11 (2%), der blev behandlet med kombinationsbehandlingen, hvilket markerede en reduktion på 70%. Der var 10 dødsfald, og alle var patienter i placebogruppen.
FDA siger, at mennesker med "alvorlige, langvarige (kroniske) medicinske tilstande" som hjertesygdomme, lungesygdomme og diabetes "synes at have større risiko for at blive indlagt på grund af COVID-19."
Dette er ikke den første monoklonale antistofbehandling, der er godkendt til brug af FDA. Agenturet tildelte en EUA til bamlanivimab alene i november.
Bamlanivimab "viste sig at være effektiv til at reducere hospitalsindlæggelsesrater blandt patienter med høj risiko for sygdomsprogression, hvis de blev brugt tidligt i sygdommen," Sunanda Gaur, MD, direktør for Clinical Research Center ved Rutgers Robert Wood Johnson Medical School i New Jersey, fortæller Verywell.
Gaur siger, at resultaterne fra forsøget er "lovende", men påpeger, at de fulde data endnu ikke er tilgængelige. Alligevel siger hun, at denne kombination er "potentielt mere effektiv end bamlanivimab givet alene."
Hvad det betyder for dig
Det er altid gode nyheder, når en anden behandling for COVID-19 er godkendt. Men hvis du ikke har en underliggende sundhedstilstand, er det usandsynligt, at denne behandling vil være tilgængelig for dig, hvis du får COVID-19.
Hvordan virker det?
Bamlanivimab er en monoklonal antistofterapi, der fungerer ved at binde direkte til dele af vira for at forhindre dem i at inficere en person. Bamlanivimab målretter spikesproteinet fra SARS-CoV-2, den virus, der forårsager COVID-19. Det er designet til at blokere virussens evne til at vedhæfte og komme ind i humane celler. Behandlingen leveres gennem en IV.
Etesevimab er også et monoklonalt antistof, der binder til overfladen af SARS-CoV-2-spidsproteinreceptoren. Etesevimab fungerer på samme måde som bamlanivimab og blev oprettet af det samme firma, Eli Lilly.
Ikke alle er berettigede til denne behandling. FDA siger, at kun personer i alderen 12 år og ældre, der anses for at have høj risiko for alvorlige komplikationer af virussen, kan modtage behandlingen.
Bamlanivimab og etesevimab er ikke godkendt til patienter, der er indlagt eller har behov for iltbehandling på grund af COVID-19. Monoklonale antistoffer som bamlanivimab og etesevimab kan forårsage dårligere resultater hos disse patienter, især hos dem der kræver ilt med høj strøm eller mekanisk ventilation.
Blandede følelser
Mens læger bifalder nyheden, påpeger flere, at mange i marken ikke har brugt monoklonale antistoffer. "Nogle havde ventet på yderligere beviser for effekten af disse stoffer i større kliniske forsøg," fortæller Prathit Kulkarni, MD, assisterende professor i medicin i infektionssygdomme ved Baylor College of Medicine i Texas, Verywell.
Som et resultat ”er der en generel mangel på viden om monoklonale antistoffer i det medicinske samfund,” fortæller Richard Watkins, MD, en læge til infektionssygdomme og professor i intern medicin ved Northeast Ohio Medical University, Verywell. Og, tilføjer han, "mange patienter har aldrig hørt om dem."
Kulkarni bemærker, at den seneste nødbrugsgodkendelse er baseret på resultater fra et større klinisk fase 3-forsøg.
Selve behandlingen er også mere kompliceret end blot at ordinere nogen en pille, siger Watkins og bemærker, at "der er personaleproblemer med hensyn til at give infusionerne i ambulante omgivelser."
Gaur er enig. ”Det er logistisk vanskeligt at administrere, da det kræver infusion, der kan tage flere timer,” siger hun. "Mere robuste data om fordelen ved denne fremgangsmåde ved tidlig behandling er nødvendige for at overbevise læger."
Alt i alt siger Watkins dog, at tilladelsen er lovende. ”Jeg er glad for, at læger nu får en anden terapi til at bekæmpe COVID-19,” siger han.

















-hyperlipidemia.jpg)