digicomphoto / Getty Images
Vigtigste takeaways
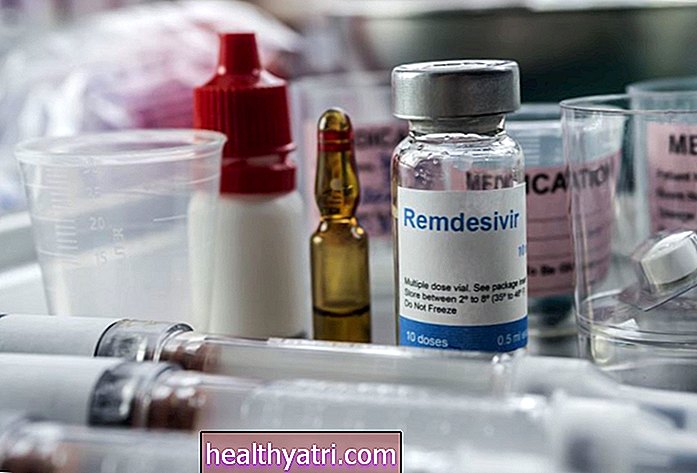
- Veklury (remdesivir) er den første FDA-godkendte behandling for mennesker med COVID-19.
- Godkendelsen er kun til behandling hos indlagte patienter over 88 pund.
- Tidligere havde lægemidlet godkendelse til nødbrug fra FDA.
Food and Drug Administration (FDA) godkendte Veklury (remdesivir) til behandling af COVID-19 hos indlagte patienter på 12 år og derover torsdag. Dette er det første officielt FDA-godkendte lægemiddel til COVID-19.
Tidligere havde FDA udstedt Emergency Use Authorization (EUA) til remdesivir, ikke fuld godkendelse. Den første EUA, der blev udstedt den 1. maj, sagde, at remdesivir kunne bruges til indlagte patienter med svær COVID-19. EUA blev genudgivet den 28. august og udvidede brugen til indlagte voksne og børn med bekræftede eller mistænkte tilfælde COVID-19, uanset deres sværhedsgrad af sygdommen.
Selvom stoffet nu er godkendt, gælder godkendelsen ikke for alle grupper. Patienter skal veje mindst 40 kg (ca. 88 pund) for at få remdesivir. I et forsøg på fortsat at tilbyde lægemidlet til pædiatriske patienter, der er omfattet af den første EUA, når det er nødvendigt, har FDA genudgiveten andenEUA til remdesiver-brug i:
- Indlagte hospitalspædiatriske patienter, der vejer 3,5 kg til mindre end 40 kg
- Indlagte hospitalspædiatriske patienter under 12 år, der vejer mindst 3,5 kg
"FDA er forpligtet til at fremskynde udviklingen og tilgængeligheden af COVID-19-behandlinger under denne hidtil usete folkesundhedsnød," sagde FDA-kommissær Stephen M. Hahn, MD i en erklæring. ”Dagens godkendelse understøttes af data fra flere kliniske forsøg, som agenturet har vurderet grundigt og repræsenterer en vigtig videnskabelig milepæl i COVID-19-pandemien. Som en del af FDAs Coronavirus Treatment Acceleration Program vil agenturet fortsætte med at hjælpe med at flytte nye medicinske produkter til patienter så hurtigt som muligt, samtidig med at det afgør, om de er effektive, og om deres fordele opvejer deres risici. ”
Hvad er Remdesivir?
Remdesivir er et direktevirkende antiviralt lægemiddel, der hæmmer viral ribonukleinsyre (RNA) syntese. Coronavirus, inklusive SARS-CoV-2, er en familie af enkeltstrenget RNA-genom. Det er bevist, at Remdesivir forhindrer disse vira i at replikere.
Remdesivir og COVID-19
Remdesivir skabte først overskrifter i foråret, da Texas-forskere identificerede det intravenøse lægemiddel som "den mest lovende behandling" for COVID-19 på trods af begrænsede kliniske data.
Da SARS-CoV-2 opstod, så forskerne lovende resultater efter test af remdesivir på virussen i et laboratorium, og kliniske forsøg begyndte kort tid derefter, forklarer Matthew D. Hall, ph.d., der arbejder ved National Center for Advancing Translational Sciences på National Institutter for sundhed. Han hjalp med at lave COVID-19 OpenData Portal til at dele COVID-19-relaterede lægemiddelreparationsdata og eksperimenter for alle godkendte lægemidler.
”De fleste godkendte lægemidler tager i gennemsnit 15 år og et par milliarder dollars at udvikle,” fortæller Hall Verywell. ”Men vi havde ikke 15 år; vi havde ikke engang 15 uger. "
Hall siger, at han og hans team fik til opgave at evaluere eksisterende ressourcer.
"Vi havde brug for at se os omkring efter de ting, der allerede var tilgængelige for os, som enten var godkendt til behandling af andre sygdomme eller blev udviklet til behandling af andre sygdomme," siger han. "De er muligvis ikke godkendt endnu, men forhåbentlig har de været hos mennesker, og vi ved, at de er sikre. Vi er heldige nok til at have masser af antivirale lægemidler. Af de lægemidler, der er godkendt, eller lægemiddelkandidater, ser remdesivir ud til har været den mest aktive, hvorfor det kunne flyttes til kliniske forsøg virkelig hurtigt. ”
Matthew D. Hall, ph.d.
De fleste godkendte stoffer tager i gennemsnit 15 år og et par milliarder dollars at udvikle. Men vi havde ikke 15 år; vi havde ikke engang 15 uger.
- Matthew D. Hall, ph.d.FDA tildelte oprindeligt en EUA den 1. maj for at gøre det muligt at behandle indlagte voksne patienter med svær COVID-19 med remdesivir. En person med svær COVID-19 blev defineret som:
- En patient med iltmætning mindre end eller lig med 94%
- En patient, der har brug for supplerende ilt
- En patient, der har behov for mekanisk ventilation
- En patient, der kræver ekstracorporeal membranoxygenering
Den udvidede EUA hjalp med at gøre lægemidlet tilgængeligt for patienter på tidligere stadier eller med mildere tilfælde af sygdommen, og godkendelsen skulle kun øge dets tilgængelighed. Hall siger, at patienter ikke behøver at blive registreret som en del af et klinisk spor for at modtage behandling, hvilket øger adgangen til mennesker, der bor i landdistrikter, der ikke bor i nærheden af forskningsfaciliteter.
”Jeg tror, at vi alle er enige om, at det ville være godt for folk, der bare er lidt dårlige derhjemme, kunne tage en antiviral middel til at udrydde virussen fra deres kroppe hurtigere for at sikre, at de ikke bliver sygere senere,” siger Hall. ”Lige nu skal du vente, indtil du er syg nok til at være på hospitalet for at få remdesivir. Det ville være dejligt at sikre, at disse mennesker aldrig er syge nok til at gå på hospitalet ved at give dem en antiviral tidligere som Tamiflu til influenza, (hvor) du går til lægen, får pillen, og det vil forkorte den tid, du er syg for. ”
Udvikling af Remdesivir
Remdesivir blev oprindeligt udviklet som en del af et samarbejde mellem Gilead Sciences, de amerikanske centre for sygdomsbekæmpelse og forebyggelse og US Army Medical Research Institute of Infectious Diseases. Det blev undersøgt som et potentielt terapeutisk middel under den vestafrikanske ebolavirusepidemi og for to andre coronavirus: alvorligt akut respiratorisk syndrom (SARS) og Mellemøsten respiratorisk syndrom (MERS).
Hvem skal tage Remdesivir?
Remdesivirs optimale patientpopulation, dosering og behandlingsvarighed er ikke kendt. I et faktaark til sundhedsudbydere tilbyder FDA følgende anbefalinger:
- For voksne og pædiatriske patienter, der vejer 40 kg og derover, er den anbefalede dosis 200 mg på dag 1 efterfulgt af efterfølgende doser på 100 mg.
- For pædiatriske patienter, der vejer mellem 3,5 kg og 40 kg, er den anbefalede dosis 5 mg / kg på dag 1 efterfulgt af efterfølgende doser på 2,5 mg / kg.
- For patienter, der ikke har behov for invasiv mekanisk ventilation og / eller iltning af ekstrakorporal membran, er den anbefalede samlede behandlingsvarighed 5 dage.
- For patienter, der har brug for invasiv mekanisk ventilation og / eller iltning af ekstrakorporal membran, er den anbefalede samlede behandlingsvarighed 10 dage.
- Hvis en patient ikke demonstrerer klinisk forbedring, kan behandlingen forlænges i op til yderligere 5 dage i en samlet behandlingsvarighed på op til 10 dage.
Gilead Sciences arbejder på at opskalere produktion og distribution af remdesivir, der betragtes som et undersøgelsesmedicin og i øjeblikket ikke er godkendt til nogen indikation.
Kliniske forsøg og foreløbige fund
FDAs beslutning om at godkende remdesivir er baseret på forskningsresultater fra et par kliniske forsøg og er blevet mødt med blandede meninger fra det medicinske samfund.
"Hvad jeg synes om ethvert lægemiddel eller enhver lægemiddelkandidat betyder ikke rigtig noget," siger Hall. ”Det, der virkelig betyder noget, er data fra et velkontrolleret klinisk forsøg. FDA ville ikke have udvidet anvendelsesområdet for EUA, hvis de ikke troede, at der ville være fordel for flere patienter. "
I en undersøgelse offentliggjort den 29. april iThe Lancet,en gruppe læger og forskere gennemførte et randomiseret, dobbeltblindet, placebokontrolleret forsøg med 237 voksne patienter med svær COVID-19 på 10 hospitaler i Hubei, Kina. De fandt, at remdesivir hjalp til med at fremskynde bedring.
"Selvom det ikke var statistisk signifikant, havde patienter, der fik remdesivir, en numerisk hurtigere tid til klinisk forbedring end dem, der fik placebo blandt patienter med en varighed af symptomer på 10 dage eller derunder," skriver forfatterne.
En amerikansk regeringsstøttet undersøgelse offentliggjorde sine foreløbige fund den 22. maj iNew England Journal of Medicinefra et randomiseret, dobbeltblindt placebokontrolleret forsøg med 1.063 COVID-19 patienter. Forskere fandt ud af, at dem, der fik et 10-dages remdesivir-forløb, havde en kortere restitutionstid sammenlignet med placebo - en median på 11 mod 15 dage.
"Disse foreløbige fund understøtter brugen af remdesivir til patienter, der er indlagt med COVID-19 og kræver supplerende iltbehandling," skriver forfatterne. "I betragtning af høj dødelighed trods brugen af remdesivir er det imidlertid klart, at behandling med et antiviralt lægemiddel alene sandsynligvis ikke er tilstrækkelig."
Den 21. august blev denJournal of the American Medical Associationoffentliggjorde et randomiseret fase-3-forsøg med 584 patienter indlagt med moderat COVID-19. lungebetændelse.Remdesivir-producenten Gilead Sciences sponsorerede dette forsøg på 105 hospitaler i USA, Europa og Asien. Patienter fik enten en 5-dages eller 10-dages remdesivir-kursus eller fik standardbehandling. Forskere fandt ingen forskel i resultater blandt 10-dages gruppen og ringe meningsfuld forskel blandt 5-dages gruppe.
Alle tre undersøgelser stod over for forskellige begrænsninger og havde vigtige designforskelle, så det er ikke rimeligt at skabe en sammenligning af æbler til æbler. Det rejser dog spørgsmål om replikerende fund, et kendetegn for klinisk forskning.
"Der er nu tre [randomiserede kontrolforsøg] med remdesivir hos indlagte patienter med forskellige resultater, hvilket rejser spørgsmålet om, hvorvidt forskellene er artefakter af valg af undersøgelsesdesign, herunder patientpopulationer, eller om lægemidlet er mindre effektivt end håbet," University of Pittsburgh School of Medicine forskere skrev i en lederartikel offentliggjort iJournal of the American Medical Associationden 21. august. "Det synes derfor klogt at hurtigst muligt foretage yderligere evalueringer af remdesivir i storstilet randomiserede kontrolforsøg designet til at imødegå den resterende usikkerhed og informere optimal brug."
Hvad det betyder for dig
U.S. Food and Drug Administration har givet sin første COVID-19-godkendelse til behandling til remdesivir. Hvis du er indlagt på hospitalet med et bekræftet eller mistænkt tilfælde af COVID-19, kan din sundhedsudbyder beslutte at ordinere dette lægemiddel.
Hvad er næste for Remdesivir?
Flere kliniske forsøg er i gang, ifølge Gilead Sciences-webstedet. Virksomheden er også i den første fase af udviklingen for at formulere remdesivir som en inhalator.
Hall siger, at det globale samfund er taget op til udfordringen, men søgningen efter et lægemiddel til SARS-CoV-2 er blevet forstærket af det faktum, at der ikke findes nogen lægemidler til humane coronavirus. De seneste udbrud af SARS og MERS blev bekæmpet gennem folkesundhedsforanstaltninger, ikke terapeutiske midler.
"Med remdesivir er vi super heldige, at den eksisterede," siger Hall. "Vi er heldige, at det blev udviklet til ebola. Vi er heldige, at det var tilgængeligt for at blive testet på mennesker nu. For hvis du trækker remdesivir fra ligningen, ved jeg ikke, hvad den næstbedste ting er. Der er ingen andet lægemiddel godkendt til behandling af SARS-CoV-2-infektion. ”














.jpg)