Akut myeloid (eller myelogen) leukæmi (AML) undertyper bliver bedre forstået, med nye forskningsveje, der undersøges. AML varierer meget fra person til person, og prognosen er ofte dårlig. Dette gør forskning, der kan hjælpe med at forbedre overlevelsesgraden, afgørende.
Nye fremskridt i løbet af de sidste mange år forbedrer diagnostik, behandlinger og overlevelsesrater, som alle giver et mere håbefuldt udsyn.
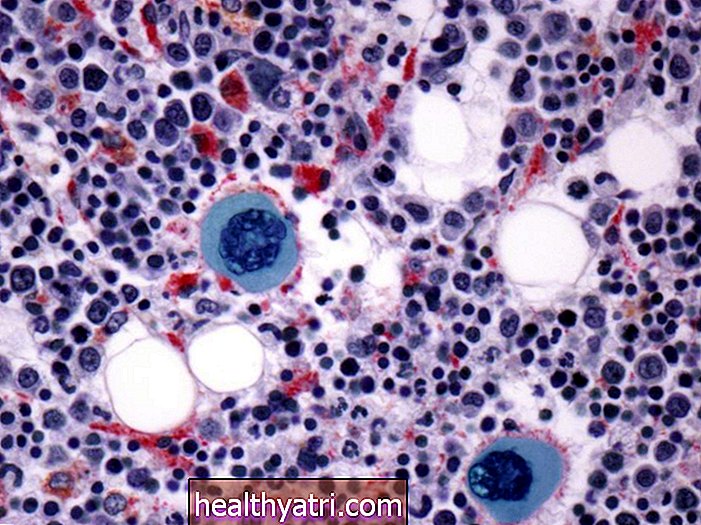
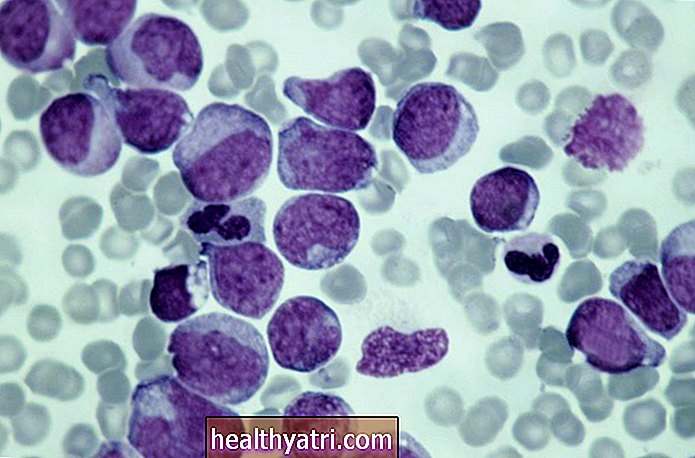
AML er en kræft i blodet og knoglemarven (de svampede indersider af knogler, hvor der fremstilles blodlegemer). Det er "akut", fordi det skrider frem hurtigt. "Myeloid" betyder, at det involverer myeloidceller, som udvikler sig til forskellige typer blodlegemer (f.eks. Røde og hvide blodlegemer, blodplader).
Albina Gavrilovic / Getty Images
Symptomer på AML inkluderer:
- Feber
- Knoglesmerter
- Sløvhed og træthed
- Hyppige infektioner
- Let blå mærker
- Usædvanlig blødning
Undertyper vs. iscenesættelse
Når de fleste kræftformer diagnosticeres, er de "iscenesat". Scenen fortæller dig, hvor avanceret kræften er, bestemmer din prognose og kan styre beslutninger om behandling.
AML er ikke iscenesat. I stedet afhænger dit syn og din behandling af din undertype, som bestemmes af laboratorietests.
De fleste AML-undertyper defineres delvist af, hvordan udviklede og unormale kræftceller ser ud under et mikroskop, når sygdommen først diagnosticeres. Derudover forstærkes AML-klassifikationen nu af nye opdagelser om genetiske ændringer eller mutationer, der er involveret.
To AML-klassificeringssystemer er i øjeblikket i brug:
- Den fransk-amerikanske-britiske (FAB) klassifikation
- Verdenssundhedsorganisationens (WHO) klassifikation
Yderligere klassificering efter komplekse genetiske undertyper udvikler sig takket være en banebrydende undersøgelse offentliggjort i 2016.
Hvorfor undertype er vigtig
At kende den genetiske sammensætning af din leukæmi kan hjælpe din læge med at forudsige, om aktuelle behandlinger ville være effektive. Dette har allerede foretaget en mere omfattende genetisk test på tidspunktet for diagnosticeringsrutinen.
Forståelse af undertyper kan også hjælpe forskere med at designe nye kliniske forsøg til at udvikle de bedste behandlinger til hver AML-type.
Klassificering af AML-undertyper
FAB-klassificeringssystemet har eksisteret siden 1970'erne, men undertypeprocessen har ændret sig et par gange i de seneste år. WHO-klassificeringssystemet blev standard i 2008 og grupperede mennesker baseret på genetiske ændringer, der ligger til grund for deres kræft (kaldet "drivermutationer").
Derefter, i 2016, kom der afgørende forskning ud iNew England Journal of Medicine (NEJM)der har taget undertypning endnu længere.
Denne undersøgelse viste, at WHO's molekylære klassifikationer ikke fungerer godt i næsten halvdelen af AML-tilfælde - 48% af deltagerne i undersøgelsen kunne ikke klassificeres baseret på WHO's molekylære grupper, selvom 96% af dem havde drivermutationer.
Efterforskere er nu begyndt at revurdere genomisk klassificering af AML fra begyndelsen baseret på:
- Opdagelsen af mange nye leukæmigener
- Opdagelsen af flere driver-mutationer pr. Patient
- Komplekse mutationsmønstre
FAB-klassificering af AML
For mere end 40 år siden delte en gruppe franske, amerikanske og britiske leukæmieksperter AML i undertyper M0 til M7 baseret på den celletype, leukæmi udvikler sig fra, og hvor modne cellerne er.
- M0 til M5 starter alle i umodne former for hvide blodlegemer.
- M6 starter i meget umodne former for røde blodlegemer.
- M7 starter i umodne former for celler, der danner blodplader.
WHO-klassificering af AML
FAB-klassificeringssystemet bruges stadig almindeligt til at gruppere AML i undertyper; dog er viden udviklet med hensyn til faktorer, der påvirker prognose og udsigter for forskellige typer AML.
Nogle af disse fremskridt blev afspejlet i World Health Organization (WHO) -systemet fra 2008, som opdeler AML i flere grupper:
- AML med myelodysplasi-relaterede ændringer
- AML relateret til tidligere kemoterapi eller stråling
- Myeloid sarkom (også kendt som granulocytisk sarkom eller klorom)
- Myeloid spredning relateret til Downs syndrom
- AML med kromosomale translokationer og inversioner
- AML ikke andetsteds specificeret
- Udifferentierede og bifenotypiske akutte leukæmier
Grupper 5, 6 og 7 er yderligere opdelt.
AML med kromosomale translokationer og inversioner
I kromosomale translokationer bryder en del af det genetiske materiale af sin oprindelige placering og binder sig igen til et andet kromosom. I inversioner kommer et segment ud, vender på hovedet og fastgør igen til dets oprindelige kromosom.
Mindst syv typer AML inkluderer translokationer, inversioner eller lignende genetiske abnormiteter.
AML ikke andetsteds specificeret
Tilfælde af AML, der ikke falder ind i en af ovenstående grupper, klassificeres på samme måde som FAB-systemet.
Udifferentierede og bifenotypiske akutte leukæmier
Disse er leukæmier, der har både lymfocytiske og myeloid egenskaber. De kaldes undertiden:
- Akut lymfocytisk leukæmi (ALL) med myeloide markører
- AML med lymfoide markører
- Blandet akut leukæmi
Nye klassifikationer: NEJM-undersøgelsen
2016-undersøgelsen, der fik den seneste ændring, omfattede 1.540 personer med AML. Forskere analyserede 111 gener, der vides at forårsage leukæmi, med det formål at identificere ”genetiske temaer” bag udviklingen af sygdommen.
De fandt ud af, at deltagerne kunne opdeles i mindst 11 hovedgrupper, hver med forskellige klynger af genetiske ændringer og med forskellige sygdomskarakteristika og træk.
Ifølge undersøgelsen havde de fleste mennesker en unik kombination af genetiske ændringer, der kørte deres leukæmi, hvilket kan hjælpe med at forklare, hvorfor AML-overlevelsesgraden varierer meget. Således arbejdede forskerne med at udvikle et nyt AML-klassificeringssystem ved hjælp af denne nye information.
De konkluderede, at der findes tre undergrupper, der ikke blev taget højde for i WHO-klassificeringssystemet. De kaldes:
- Kromatin-spliceosom
- TP53-aneuploidi
- IDH2R172
Brug af det foreslåede system til at klassificere de 1.540 deltagere i undersøgelsen:
- 1.236 mennesker med drivermutationer kunne hver klassificeres i en enkelt undergruppe
- 56 patienter opfyldte kriterierne for to eller flere undergrupper
- 166 mennesker med chaufførmutationer forblev uklassificerede
Forfatterne anbefalede, at fem specifikke genetiske typer (kaldet TP53, SRSF2, ASXL1, DNMT3A og IDH2) på kort sigt skulle indarbejdes i prognostiske retningslinjer, fordi de er almindelige og har stor indflydelse på resultaterne.
Prognostic vs Diagnostic
NEJM-forskerne opfordrede til to separate klassificeringssystemer:
- En til brug ved diagnosticering af mennesker
- Én til anvendelse til forudsigelse af resultater (prognose)
De siger, at det diagnostiske system skal være baseret på faste egenskaber, mens det prognostiske system bør ændre sig regelmæssigt baseret på tilgængelige behandlinger.
Nyere forskning
Baseret stort set på NEJM-undersøgelsen har andre forskere undersøgt visse genetiske profiler af AML. Ifølge undersøgelser offentliggjort i 2020 har nogle forskere identificeret:
- Potentielle nye tidlige diagnostiske metoder til visse undertyper
- Potentielle nye måder at identificere mennesker, der sandsynligvis er resistente over for lægemidler
- Potentielle nye kombinationer af behandlinger for lægemiddelresistente tilfælde
En undersøgelse identificerede et nyt lægemiddel, som forskere siger er effektivt mod lægemiddelresistente AML-undertyper, og "når det er i brug," vil det have en øjeblikkelig klinisk effekt. "
Diagnosticering af AML-undertyper
Læger har mange værktøjer til at diagnosticere AML og bestemme din undertype. Diagnosen starter med en fysisk eksamen. Under din eksamen vil de lede efter tegn som:
- Omfattende blå mærker
- Blødende
- Infektion
- Abnormiteter i dine øjne, mund, lever, milt eller lymfeknuder
For at bekræfte en formodet AML-diagnose kan de bestille enhver kombination af følgende tests:
- Komplet blodtal (CBC)
- Knoglemarvsaspiration
- Knoglemarvsbiopsi
- Lændepunktur
- Billedbehandlingstest (f.eks. Røntgen, CT-scanning, MR)
- Cytogenetik
Cytogenetik og molekylær test er især vigtig for at bestemme din undertype. Det indebærer at undersøge din celles genetiske materiale under et mikroskop for at lede efter genetiske abnormiteter, såsom translokationer og inversioner.
Diagnosticering af leukæmiUndertyper og AML-behandling
Et væld af nye AML-lægemidler er blevet godkendt af Food and Drug Administration i de sidste par år; dog var de alle under udvikling i god tid inden 2016-forskningen kom ud.
Nu, i vid udstrækning baseret på denne forskning, undersøges i øjeblikket mange potentielle behandlinger for AML baseret på specifikke genetiske undertyper.
Flere undersøgelsesmedicin, der er målrettet mod bestemte genetiske mutationer, er begyndt i forskningsprocessen, og forskere ser også på nye typer kemoterapimedicin, lægemiddel- og antistofkombinationer og lægemidler kaldet kinasehæmmere.
Nogle af disse lægemidler er allerede på markedet for andre forhold, mens andre viser lovende resultater i forsøg. For eksempel:
- Potentielle behandlinger for en AML-mutation kaldet TET2 kan omfatte lægemidler kaldet PARP-hæmmere eller HMA'er kombineret med C-vitamin.
- En gruppe enzymer kaldet KAT'er kan hjælpe med at behandle AML med mutationer i gener kaldet EP300 og CBP.
- Narkotika kaldet p300-aktivatorer undersøges i AML-dyremodeller.
Flere andre AML-genetiske undertyper undersøges, så forskere kan finde ud af, hvilke lægemidler der kan målrette mod dem.
Behandlingsmuligheder for leukæmiEt ord fra Verywell
Akut myeloid leukæmi har altid været en skræmmende diagnose med dårlige udsigter.
Men med nye lægemidler til rådighed, mere på vej og konstante nye opdagelser om genetiske undertyper, forbedres prognosen og vil sandsynligvis fortsætte med at gøre det.