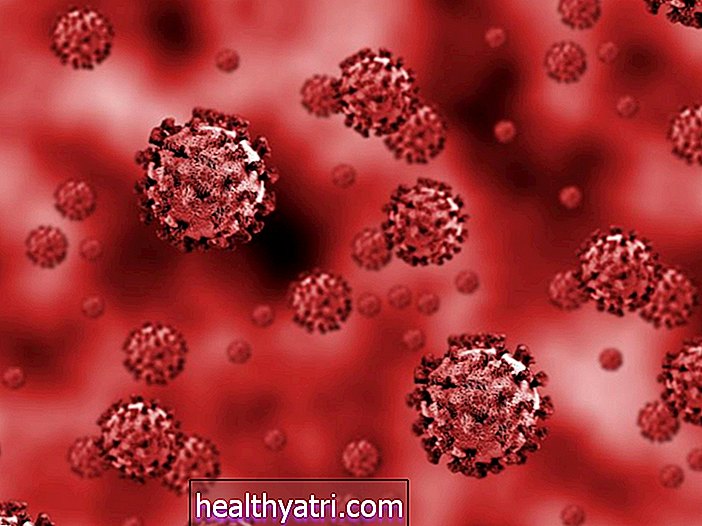
Interessen for en vaccine mod urinvejsinfektioner (UTI'er) strækker sig tilbage til 1950'erne, og siden da har forskere ledt efter en levedygtig kandidat til at forhindre bakterierneEscherichia coli.(E coli) fra kolonisering af blæren og etablering af en infektion.
I juli 2017 tildelte den amerikanske fødevare- og lægemiddeladministration (FDA) Sequoia Sciences 'FimH UTI-vaccine hurtig betegnelse. Hvis den er godkendt, vil vaccinen blive den første vaccine, der er godkendt til behandling af UTI'er i USA.
Blend_ImagesCLOSED / Getty ImagesFast-track er en proces designet til at fremskynde udviklingen og gennemgangen af lægemidler, der behandler alvorlige tilstande og udfylder et udækket medicinsk behov.
Om UTI'er
Parallelt med den udbredte anvendelse af antibiotika har der været en stigning i antallet af antibiotikaresistente bakterier, der forårsager svære UTI'er. Når dette sker, kan infektionen stige fra blæren (hvor det kaldes blærebetændelse) ind i nyrerne (forårsager pyelonefritis).
I nogle tilfælde kan infektionen yderligere sprede sig i blodet og forårsage sepsis. Nyreskader, hospitalsindlæggelse og endda død er konsekvenser af en alvorlig, ubehandlet UTI-infektion.
I lyset af denne trussel har der været stigende interesse for at udvikle en vaccine, der undgår behovet for antibiotika. Dette er især vigtigt for kvinder, der oplever tilbagevendende eller kroniske urinvejsinfektioner, der har større risiko for multiresistens.
UTI er en af de hyppigste kliniske bakterielle infektioner hos kvinder og tegner sig for næsten 25% af alle infektioner.
Om FimCH-vaccinen
FimH-vaccinen er en specifik antigenvaccine. Dette er en vaccine, der indeholder et protein - i dette tilfælde FimH-bakterieadhæsionsproteinet - som kroppen genkender som skadelig. Som reaktion vil immunsystemet producere antistoffer designet til at kontrollere den specifikke organisme.
FimH-proteinet fungerer ved at levereE colimidlerne til at fastgøre til celler på blæreoverfladen. Ved at gøre det kan bakterierne kolonisere og sprede sig. Uden FimH-proteinetE coliville være dårligt rustet til at gøre dette.
På grund af fremskridt inden for DNA-teknologi er specifikke antigenvacciner blevet populære vaccinemodeller for vaccineudvikling sammenlignet med mere traditionelle heldræbte vacciner eller inaktiverede vacciner.
Tidlige fase forsøgsresultater
FimH-vaccinen er ikke ny. Det blev oprindeligt licenseret af MedImmune (et helejet datterselskab af AstraZeneca) i slutningen af 1990'erne og gik ind i fase 1 og fase 2 kliniske forsøg, før det blev droppet fra udvikling.
Sequoia Sciences licenserede derefter vaccinen, ændrede adjuvansen (et stof, der styrker immunresponset) og gik i gang med egne forsøg. De tidlige resultater har været positive.
Af de 67 kvinder, der var tilmeldt denne første undersøgelse, havde 30 en to-årig historie med tilbagevendende UTI'er, mens de resterende 37 ikke havde nogen historie med UTI'er. Alderen varierede fra 18 til 64.
Kvinderne blev opdelt i grupper og fik forskellige injektioner, hvoraf nogle involverede 50 mikrogram (µg) af FimH-vaccinen adjuvanseret med forskellige doser af et syntetisk lipid kaldet PHAD. Andre fik en ikke-adjuveret vaccine eller placebo.
Vaccinen blev injiceret i deltoidmusklen i overarmen i løbet af 180 dage. Fire vaccinationer blev givet i alt (dag 1, 31, 90 og 180).
Ved afslutningen af forsøgsperioden havde kvinder, der fik den adjuverede vaccine, en 10 gange stigning i FimH-antistof, hvilket antydede et stærkt immunforsvar.
Samlet set blev vaccinen sagt at være veltolereret og at have genereret en robust nok immunrespons til at berettige FDA's hurtige betegnelse
Selvom fase 1-undersøgelsen blev afsluttet i 2017, blev resultaterne kun offentliggjort i deres helhed i januar 2021-udgaven afHumane vacciner og immunterapier.
Forskning er i gang.
Andre kandidater til vaccinen
Janssen Pharmaceuticals og GlycoVaxyn har også arbejdet på en anden UTI-vaccine kaldet ExPEC4V. I modsætning til Sequoia Sciences-vaccinen er ExPEC4V-vaccinen en konjugeret vaccine. Dette er en vaccine, der smelter (konjugerer) antigenet til et bærermolekyle for at øge dets stabilitet og effektivitet.
Fase 1-forsøget involverede 188 kvinder, hvoraf 93 fik vaccinen og 95 af dem fik placebo. Deltagerne var mellem 18 og 70. Alle havde en historie med tilbagevendende UTI'er.
Ifølge forskerne blev ExPEC4V-vaccinen veltolereret og induceret et signifikant immunrespons, hvilket resulterede i færre UTI'er forårsaget afE coli.
Fase 2-resultater var også relativt positive. I denne fase af undersøgelsen blev der givet to injektioner: en på den første dag i forsøget og en anden 180 dage senere.
Ifølge forskning offentliggjort iÅbent forum smitsomme sygdomme,kvinder, der modtog ExPEC4V-vaccinen, havde en fordobling af antistofresponset sammenlignet med dem, der fik placebo, som ikke havde nogen.
Bivirkningerne var generelt milde til moderate (hovedsageligt træthed og smerter ved injektionsstedet), selvom de forekom med dobbelt så høj hastighed i vaccinegruppen som placebogruppen.
Forskning er i gang.
Et ord fra Verywell
Kvinder, der oplever tilbagevendende UTI'er, vil sandsynligvis være ideelle kandidater til en UTI-vaccine, hvis en godkendes. Gentagen brug af antibiotika hos kvinder med kroniske infektioner øger kun risikoen for multiresistens, både individuelt og inden for den større befolkning.
Indtil der er vaccine tilgængelig, skal du kontakte en specialist kaldet urolog, hvis du oplever tilbagevendende urinvejsinfektioner. Og vigtigere er det, at du ikke anmoder om et antibiotikum, hvis et ikke tilbydes. Begrænset anvendelse hjælper med at forhindre udviklingen af antibiotikaresistente bakteriestammer.
Førende sundhedsorganisationer, herunder Centers for Disease Control and Prevention the World Health Organization, har erklæret antibiotikaresistens som en af de mest alvorlige sundhedstrusler, som verden står over for i dag.









-overview.jpg)